Soutenance de thèse de Baptiste Martin : Dispersions aqueuses d'organogel pour la délivrance orale de substances actives
Vendredi 31 mars à 9h30 - Maison de la Recherche et de la Valorisation / Amphithéatre 3
Après 3 années de recherches passées au sein du laboratoire, Baptiste soutient sa thèse intitulée : Dispersions aqueuses d'organogel pour la délivrance orale de substances actives
Ces travaux de thèse ont porté sur l’utilisation d’un nouveau type de dispersion colloïdale pour l’encapsulation et la délivrance orale de substance active (SA). Les dispersions aqueuses d’organogel, nommées "dispersions de gélosomes", sont des systèmes lipidiques semi-solides, intermédiaires entre les nanoémulsions et les nanoparticules lipidiques solides, qui constituent des véhicules prometteurs pour la solubilisation de composés hydrophobes. Les dispersions de gélosomes sont préparées par dispersion à chaud d’un organogel, composé d’une huile et d’un gélifiant lipophile de bas poids moléculaire (acide 12-hydroxystéarique : HSA), formant des gouttelettes d’émulsion en présence d’alcool polyvinylique hydrolysé à 80% (PVA80) et qui conduisent à des nanoparticules d’organogel après refroidissement.
Dans une première partie, des études de physico-chimie ont permis de sélectionner la formulation de de gélosomes la plus adaptée, en évaluant l’influence de la proportion de chaque constituant sur la taille et la stabilité des dispersions.
Une deuxième partie a porté sur l’encapsulation de SA lipophiles dans les dispersions de gélosomes. L’incorporation de SA lipophiles (indométacine, kétoconazole, ibuprofène, éfavirenz) n’a pas altéré la stabilité des dispersions et un très bon taux d’encapsulation a été obtenu (>98%). Les études de libération par dialyse ont montré un profil de libération immédiate, liée à une diffusion rapide de la SA hors des gélosomes.
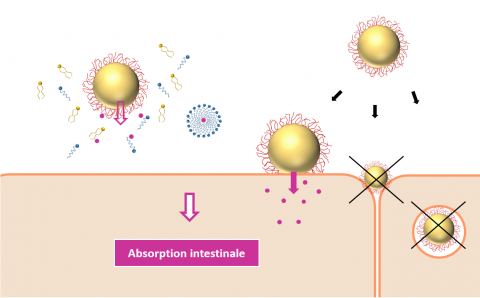
Enfin, une troisième partie était consacrée à l’évaluation biopharmaceutique de dispersions de gélosomes chargées en éfavirenz en vue d’une administration orale. Une étude pharmacocinétique in vivo a montré l’intérêt des gélosomes pour améliorer la biodisponibilité de l’éfavirenz comparativement à une suspension de SA. Elle s’explique par une mise à disposition rapide de la SA dissoute dans le gélosome au niveau de la muqueuse jéjunale favorable à l’absorption, combinée à la surface d’échange très importante des dispersions submicroniques de gélosomes. L’étude du mécanisme d’absorption in vitro sur modèle cellulaire Caco-2 ont par ailleurs montré l’absence de passage des gélosomes par endocytose ou voie paracellulaire, et une prédominance des mécanismes de diffusion passive transcellulaire.


